Vaksin Sinovac Paling Lambat Disetujui WHO, Ternyata Ini Prosesnya
Photo
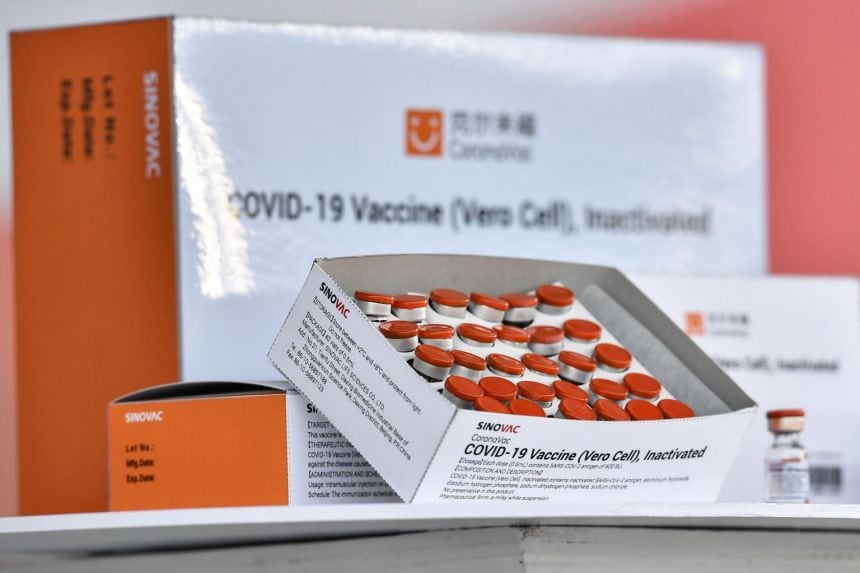
JawaPos.com - Organisasi Kesehatan Dunia (WHO) sudah memvalidasi vaksin Sinovac untuk penggunaan darurat. Kemudian memberikan jaminan kepada negara, penyandang dana, lembaga pengadaan, dan masyarakat bahwa vaksin itu memenuhi standar internasional untuk keamanan, kemanjuran, dan pembuatan. Vaksin ini diproduksi oleh perusahaan farmasi Sinovac yang berbasis di Beijing. Sinovac adalah vaksin terakhir yang disetujui, dan paling lambat mendapat persetujuan WHO setelah Sinopharm.
“Dunia sangat membutuhkan beberapa vaksin Covid-19 untuk mengatasi kesenjangan akses yang sangat besar di seluruh dunia,” kata Asisten Direktur Jenderal WHO untuk Akses ke Produk Kesehatan dr. Mariangela Simao,
“Kami mendesak produsen untuk berpartisipasi dalam Fasilitas COVAX, berbagi pengetahuan dan data mereka, serta berkontribusi untuk mengendalikan pandemi," katanya.
Alur Persetujuan Vaksin
Daftar Penggunaan Darurat (EUL) WHO merupakan prasyarat untuk pasokan vaksin Fasilitas COVAX dan pengadaan internasional. Ini juga memungkinkan negara untuk mempercepat persetujuan peraturan mereka sendiri untuk mengimpor dan mengelola vaksin Covid-19.
EUL menilai kualitas, keamanan, dan kemanjuran vaksin Covid-19, serta rencana manajemen risiko dan kesesuaian program, seperti persyaratan rantai dingin. Penilaian dilakukan oleh kelompok evaluasi produk, yang terdiri dari ahli regulasi dari seluruh dunia dan Kelompok Penasihat Teknis (TAG), yang bertanggung jawab melakukan penilaian risiko-manfaat untuk rekomendasi independen, tentang apakah vaksin dapat didaftarkan untuk penggunaan darurat. Dan, dalam kondisi apa.
Baca juga: Singapura Izinkan Sinovac tapi Tak Gratis, Klinik Swasta Berebut
"Dalam kasus vaksin Sinovac-CoronaVac, penilaian WHO mencakup inspeksi di tempat fasilitas produksi," kata pernyataan resmi WHO.
Produk Sinovac-CoronaVac adalah vaksin yang tidak aktif. Persyaratan penyimpanannya yang mudah membuatnya sangat mudah dikelola dan sangat cocok untuk pengaturan sumber daya rendah.
Kelompok Ahli Penasihat Strategis WHO tentang Imunisasi (SAGE) juga telah menyelesaikan tinjauannya terhadap vaksin tersebut. Berdasarkan bukti yang ada, WHO merekomendasikan vaksin untuk digunakan pada orang dewasa berusia 18 tahun ke atas, dalam jadwal dua dosis dengan jarak dua hingga empat minggu.
Hasil efikasi vaksin menunjukkan bahwa vaksin mencegah penyakit simtomatik pada 51 persen dari mereka yang divaksinasi dan mencegah Covid-19 yang parah dan rawat inap pada 100 persen dari populasi yang diteliti.
Beberapa orang dewasa yang lebih tua (lebih dari 60 tahun) terdaftar dalam uji klinis, sehingga kemanjuran tidak dapat diperkirakan pada kelompok usia ini. Namun demikian, WHO tidak merekomendasikan batas usia atas untuk vaksin karena data yang dikumpulkan selama penggunaan selanjutnya di banyak negara dan data imunogenisitas yang mendukung menunjukkan bahwa vaksin tersebut kemungkinan memiliki efek perlindungan pada orang tua.
"WHO merekomendasikan bahwa negara-negara yang menggunakan vaksin pada kelompok usia yang lebih tua melakukan pemantauan keamanan dan efektivitas untuk memverifikasi dampak yang diharapkan dan berkontribusi untuk membuat rekomendasi lebih kuat untuk semua negara," kata WHO.
Ketatnya Alur Pendaftaran
Prosedur Daftar Penggunaan Darurat (EUL) menilai kesesuaian produk kesehatan baru selama keadaan darurat kesehatan masyarakat. Tujuannya adalah untuk membuat obat-obatan, vaksin dan diagnostik tersedia secepat mungkin untuk mengatasi keadaan darurat, sambil mematuhi kriteria keamanan, kemanjuran dan kualitas yang ketat.
Penilaian mempertimbangkan ancaman yang ditimbulkan oleh keadaan darurat serta manfaat yang akan diperoleh dari penggunaan produk terhadap potensi risiko apa pun. Jalur EUL melibatkan penilaian yang ketat terhadap data uji klinis fase II dan fase III akhir serta data tambahan substansial tentang keamanan, kemanjuran, kualitas, dan rencana manajemen risiko dengan fokus pada kebutuhan negara berpenghasilan rendah dan menengah. Data ini ditinjau oleh para ahli independen dan tim WHO yang mempertimbangkan bukti terkini tentang vaksin yang sedang dipertimbangkan, rencana untuk memantau penggunaannya, dan rencana untuk studi lebih lanjut.
Sebagai bagian dari proses EUL, perusahaan yang memproduksi vaksin harus berkomitmen untuk terus menghasilkan data untuk memungkinkan lisensi penuh dan prakualifikasi vaksin oleh WHO. Proses prakualifikasi WHO akan menilai data klinis tambahan yang dihasilkan dari uji coba dan penyebaran vaksin secara bergilir untuk memastikan vaksin memenuhi standar kualitas, keamanan, dan kemanjuran yang diperlukan untuk ketersediaan yang lebih luas.
Disetujui SAGE
Lalu, vaksin dinilai oleh SAGE. SAGE adalah kelompok penasihat utama WHO untuk vaksin dan imunisasi. Badan ini bertugas memberi nasihat kepada WHO tentang kebijakan dan strategi global secara keseluruhan, mulai dari vaksin dan teknologi imunisasi, penelitian dan pengembangan, hingga pemberian imunisasi dan keterkaitannya dengan intervensi kesehatan lainnya. SAGE tidak hanya peduli dengan vaksin dan imunisasi masa kanak-kanak, tetapi semua penyakit yang dapat dicegah dengan vaksin.
SAGE menilai bukti tentang keamanan, kemanjuran, efektivitas, dampak dan kesesuaian program, dengan mempertimbangkan dampak kesehatan individu dan masyarakat. Rekomendasi SAGE Interim untuk produk EUL memberikan panduan bagi pembuat kebijakan vaksinasi nasional. Rekomendasi ini diperbarui saat bukti tambahan tersedia dan karena ada perubahan epidemiologi penyakit dan ketersediaan vaksin tambahan dan intervensi pengendalian penyakit lainnya.
Tags
Artikel Terkait
Terpopuler

50 Unit Mobil Koperasi Desa Merah Putih Tiba di Wonogiri, Dandim 0728/Wonogiri: Saran Saya Tidak Usah Digunakan Dulu Mobilnya
7 Tahun Tak Terkalahkan! Bernardo Tavares Wajib Jaga Harga Diri Persebaya Surabaya di Derbi Jawa Timur Lawan Arema FC
15 Rekomendasi Restoran Terbaik Dekat Tugu Muda Semarang: Surganya Kuliner yang Wajib Dicoba Pelancong dan Wisatawan!
14 Rekomendasi Kuliner Depok untuk Keluarga, Tempat Makan Nyaman dengan Menu Beragam
Jadwal Lengkap MotoGP Spanyol 2026! Misi Berat Veda Ega Pratama dan Mario Aji dari Barisan Belakang di Jerez
Pesan Haru dari Ernando Ari! Dukungan Diam-Diam Bikin Milos Raickovic Bangkit di Persebaya Surabaya
Terdepak dari Puncak Klasemen Liga Inggris, Bayang-bayang Kegagalan Juara di Akhir Musim kembali Menghantui Arsenal
18 Rekomendasi Sarapan Pagi di Bandung Paling Sedap, Sederet Kuliner Mantap yang Wajid Disantap
Profil Agnes Aditya Rahajeng, Pemenang Puteri Indonesia 2026
Kabar Gembira! Gubernur Banten Resmi Hapus Pajak Kendaraan Bermotor, Ini Syaratnya!

- Nasional
- Haji
- Ekonomi
- Oto Dan Tekno
- Arsitektur Dan Desain
- Jawa Pos 75 Tahun
- Kabinet Merah Putih
- Features
- Jabodetabek
- Humaniora
- Islami
- Hobi & Kesenangan
- Sports
- Infrastruktur
- Zodiak
- Kepribadian
- Berita Daerah
- Entertainment
- Lifestyle
- Internasional
- Kesehatan
- Sepak Bola Indonesia
- Opini
- Surabaya Raya
- Sisi Lain
- Ternyata Hoax
- Sepak Bola Dunia
- Minggu
- Art Space
- Parenting
- Kuliner
- Karir


